La ricerca oncologica sta attraversando una fase di trasformazione profonda, nella quale il sistema immunitario non è più considerato un semplice spettatore della malattia tumorale, ma il protagonista di strategie terapeutiche sempre più sofisticate e mirate. Negli ultimi mesi, una serie di scoperte e studi clinici di rilievo internazionale hanno ridisegnato il panorama dell’immunoncologia, aprendo prospettive concrete per milioni di pazienti affetti da tumori oggi ancora difficili da trattare.
Il Nobel che ha cambiato la prospettiva
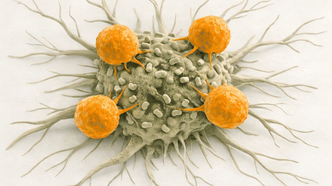
Il Premio Nobel per la Fisiologia o la Medicina 2025 ha sancito il valore scientifico di una scoperta destinata a influenzare in modo duraturo la medicina oncologica: quella dei linfociti T regolatori, noti come T-reg, cellule del sistema immunitario che, in condizioni normali, svolgono una funzione protettiva prevenendo reazioni autoimmuni, ma che all’interno del microambiente tumorale si trasformano in alleati del cancro, sopprimendo l’attività delle altre cellule immunitarie e rendendo il tumore invisibile alle difese dell’organismo. Come ha sottolineato la comunità scientifica commentando il riconoscimento, “la scoperta dei T-reg è cruciale non solo perché ha migliorato la conoscenza del sistema immunitario, ma anche per aver stimolato lo sviluppo di possibili nuove terapie mirate a inibire i T-reg nei pazienti tumorali” . In quasi un terzo dei casi in cui si sviluppa un tumore, il tessuto neoplastico riesce a costruire intorno a sé un microambiente immunosoppressorio, di cui i linfociti T-reg sono i principali artefici, neutralizzando di fatto la sorveglianza immunitaria .
I ricercatori dell’Università di Siena, attraverso studi di sequenziamento ad alta potenza per singola cellula, hanno identificato molecole che caratterizzano esclusivamente i T-reg intratumorali, sviluppando un anticorpo monoclonale diretto specificamente contro di esse, con l’obiettivo di ottenere un effetto terapeutico analogo a quello degli inibitori dei checkpoint immunitari, ma con un profilo di tossicità ridotto . Questa linea di ricerca si colloca all’interno di un approccio più ampio che mira a “sbloccare” il sistema immunitario dall’interno del tumore stesso, anziché limitarsi ad agire dall’esterno.
I vaccini mRNA: una svolta inattesa
Uno degli sviluppi più sorprendenti degli ultimi mesi riguarda il ruolo dei vaccini a mRNA anti-Covid-19 nel potenziamento dell’immunoterapia oncologica. Uno studio retrospettivo pubblicato sulla rivista Nature ha rilevato che la somministrazione di un vaccino mRNA contro il coronavirus entro 100 giorni dall’inizio di una terapia con inibitori dei checkpoint immunitari (ICI) comporta un miglioramento significativo della sopravvivenza: nei pazienti con cancro al polmone, la sopravvivenza mediana è passata da 20,6 mesi a 37,3 mesi, mentre in quelli con melanoma da 26,7 mesi a un intervallo compreso tra 30 e 40 mesi . Il meccanismo ipotizzato dagli autori coinvolge la proteina PD-L1: i vaccini mRNA ne stimolano l’espressione sulle cellule tumorali, rendendole bersagli più facilmente riconoscibili dagli anticorpi monoclonali ICI, con conseguente eliminazione selettiva delle cellule cancerose .
Questi risultati hanno alimentato un interesse crescente verso i vaccini a mRNA progettati specificamente contro i tumori, tarati sulle mutazioni individuali di ciascun paziente. Attualmente sono in corso oltre 230 trial clinici su vaccini mRNA oncologici a livello globale , tra cui studi di fase III condotti da aziende come MSD e Moderna che combinano il vaccino personalizzato con il pembrolizumab, inibitore dei checkpoint oggi tra i farmaci oncologici più utilizzati al mondo. I dati preliminari di questi studi, attesi in forma definitiva nel corso del 2026, sono stati descritti dalla comunità scientifica come “molto promettenti” .
Le cellule CAR-T e la nuova frontiera dell’ingegneria cellulare
Parallelamente all’avanzamento delle terapie basate su anticorpi monoclonali e vaccini, prosegue a ritmo sostenuto la ricerca sulle cellule CAR-T, linfociti T prelevati dal paziente e riprogrammati tramite tecniche di ingegneria genetica per riconoscere e aggredire selettivamente le cellule tumorali. Un gruppo di ricercatori dell’IRCCS Ospedale San Raffaele di Milano ha pubblicato su Science Translational Medicine i risultati di uno studio preclinico che ha sviluppato cellule CAR-T ingegnerizzate per colpire la proteina Caderina-17 (CDH17), espressa in grande quantità sulle cellule del tumore del colon-retto ma assente nei tessuti sani, aprendo così la strada a nuove speranze terapeutiche per le metastasi epatiche da carcinoma del colon . Come ha spiegato la responsabile dello studio, la dottoressa Monica Casucci, la specificità di questo approccio consente di colpire il tumore con elevata precisione, riducendo il rischio di danni agli organi sani.
L’immunoterapia cellulare di tipo CAR-T rappresenta oggi una delle direttrici di sviluppo più dinamiche dell’oncologia mondiale: si prelevano dal paziente le cellule T, le si dota tramite ingegneria genetica di recettori artificiali in grado di riconoscere antigeni specifici del tumore, e le si re-infondono nell’organismo affinché attacchino la malattia . L’obiettivo dei ricercatori è ora estendere questo approccio a tumori solidi, storicamente più difficili da trattare rispetto alle neoplasie ematologiche per le quali le terapie CAR-T hanno già ottenuto approvazione regolatoria.
L’immunoterapia neoadiuvante: prima della chirurgia
Un altro filone di ricerca che sta guadagnando consenso crescente nella comunità medica riguarda l’impiego dell’immunoterapia in fase neoadiuvante, ovvero prima dell’intervento chirurgico, con l’obiettivo di “caricare” il sistema immunitario contro il cancro prima che il bisturi venga utilizzato. I dati emersi dal trial clinico UNICORN, condotto presso l’Istituto Nazionale dei Tumori di Milano, hanno mostrato che circa il 30% dei pazienti affetti da tumore del colon-retto trattati con una combinazione innovativa di immunoterapici di nuova generazione — botensilimab e balstilimab — ha raggiunto una remissione patologica completa con la sola immunoterapia, senza necessità di intervento chirurgico . Questo risultato ha attirato l’attenzione della comunità scientifica internazionale e ha dato impulso a un progetto europeo finalizzato a comprendere perché alcuni pazienti rispondano in modo eccezionale a queste terapie.
L’approccio neoadiuvante si sta dimostrando efficace su un numero crescente di tumori: dal melanoma al carcinoma polmonare, dal cancro al seno triplo negativo a quello della vescica, le evidenze scientifiche disponibili indicano che anticipare l’immunoterapia rispetto alla chirurgia può migliorare significativamente sia l’efficacia della cura che la sopravvivenza a lungo termine . Questo cambio di sequenza terapeutica, che fino a pochi anni fa avrebbe potuto sembrare controintuitivo, riflette una comprensione più matura del modo in cui il sistema immunitario interagisce con il tumore nelle sue fasi evolutive.
Il ruolo del microbiota e le sfide future
Fra i fronti di ricerca più promettenti per il 2026 figura anche lo studio del microbiota intestinale e della sua influenza sull’efficacia delle terapie oncologiche. Secondo quanto riportato dall’AIRC, la composizione della flora batterica intestinale sembra modulare la risposta del sistema immunitario alle terapie, aprendo possibili strategie di intervento complementari, come la modulazione del microbiota per potenziare l’effetto degli inibitori dei checkpoint o dei vaccini antitumorali . Si tratta di un ambito ancora in fase esplorativa, ma che negli ultimi anni ha prodotto risultati preliminari tali da giustificare investimenti significativi in ricerca clinica.
Il quadro complessivo che emerge dall’oncologia del 2026 è quello di una disciplina in profonda trasformazione, nella quale il sistema immunitario viene progressivamente riconosciuto come lo strumento terapeutico più potente a disposizione della medicina moderna. Le sfide che rimangono aperte riguardano la resistenza di alcuni tumori all’immunoterapia, la gestione degli effetti collaterali autoimmuni delle terapie con ICI, e la necessità di identificare biomarcatori predittivi affidabili che consentano di selezionare i pazienti che beneficeranno maggiormente di ciascun approccio. Il rischio, segnalato da più parti, è che i tagli ai finanziamenti alla ricerca biomedica negli Stati Uniti possano rallentare uno slancio scientifico che, per ora, appare inarrestabile . Per restare sempre aggiornato scarica GRATIS la nostra App!